Bài 5 trang 129 sgk hóa học 12
5. Cho một lượng hỗn hợp Mg – Al tác dụng với dung dịch HCl dư thu được 8,96 lít H2. Mặt khác, cho lượng hỗn hợp như trên tác dụng với dung dịch NaOH dư thì thu được 6,72 lít H2. Các thể tích khí đều đo ở đktc.
Tính khối lượng của mỗi kim loại có trong lượng hỗn hợp đã dùng.
Hướng dẫn.
nH2 ở (1) và (2) = 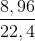 = 0,4 (mol); nH2 ở (3) =
= 0,4 (mol); nH2 ở (3) = 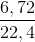 = 0,3 (mol)
= 0,3 (mol)
2Al + 6HCl → 2AlCl3 + 3H2 ↑ (1)
0,3 0,3 (mol)
Mg + 2HCl → MgCl2 + H2 ↑ (2)
0,1 0,1 (mol)
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑ (3)
0,2 0,3 (mol)
=> mMg = 21.0,1 = 2,4 (gam); mAl = 27.0,2 = 5,4 (gam).
Bài 6 trang 129 sgk hóa học 12
6. Cho 100 ml dung dịch AlCl3 1M tác dụng với 200 ml dung dịch NaOH. Kết tủa tạo thành được làm khô và nung đến khối lượng không đổi cân nặng 2,55 gam. Tính nồng độ mol của dung dịch NaOH ban đầu.
Hướng dẫn.
nAlCl3 = 0,1.1 = 0,1 (mol); nAl2O3 = \(\frac{2,55}{102}\) = 0,025 (mol)
Có hai trường hợp:
a)NaOH thiếu.
AlCl3 + 3NaOH → Al(OH)3 ↓ + 3NaCl (1)
0,05.3 0,05 (mol)
2Al(OH)3 \(\overset{t^{o}}{\rightarrow}\) Al2O3 + 3H2O (2)
0,05 0,025 (mol)
=>CM (NaOH) = \(\frac{0,15}{0,2}\) = 0,75 (M).
b) NaOH dư một phần.
AlCl3 + 3NaOH → Al(OH)3 ↓ + 3NaCl (1)
0,1 0,3 0,1 (mol)
Al(OH)3 + NaOH → NaAlO2 + 2H2O (2)
0,05 0,05 (mol)
2Al(OH)3 \(\overset{t^{o}}{\rightarrow}\) Al2O3 + 3H2O (3)
0,05 0,025 (mol)
=> nNaOH = 0,3 + 0,05 = 0,35 (mol); CM (NaOH) = \(\frac{0,35}{0,2}\) = 1,75 (M).
Bài 7 trang 129 sgk hóa học 12
7. Có 4 mẫu kim loại là Na, Al, Ca, Fe. Chỉ dùng nước làm thuốc thử thì số kim loại có thể phân biệt được tối đa là bao nhiêu?
A. 1. B. 2.
C. 3. D. 4.
Hướng dẫn.
Chọn D.
Chỉ dùng nước, có thể nhận biết được cả 4 kim loại.
Cho 4 kim loại vào nước:
-Kim loại phản ứng mạnh, giải phóng chất khí, dung dịch thu được trong suốt là Na.
-Kim loại phản ứng mạnh, giải phóng chất khí, dung dịch thu được vẩn đục là Ca vì tạo ra Ca(OH)2 ít tan.
- Dùng dung dịch NaOH thu được cho tác dụng với 2 kim loại còn lại. Kim loại nào tan được và giải phóng ra khí là Al, kim loại không phản ứng là Fe.
Bài 8 trang 129 sgk hóa học 12
Bài 8. Điện phân \(A{l_2}{O_3}\) nóng chảy với dòng điện cường độ \(9,65 A\) trong khoảng thời gian \(3000\) giây, thu được \(2,16\) gam \(Al\). Hiệu suất của quá trình điện phân là.
A. \(60\%\). B. \(70\%\).
C. \(80\%\). D. \(90\%\).
Giải
Theo định luật Faraday khối lượng nhôm thu được là:
\({m_{Al}} = {{AIt} \over {96500n}} = {{27.9,65.3000} \over {96500.3}} = 2,7(g)\)
Hiệu suất phản ứng là:
\(H = {{2,16} \over {2,7}}.100\% = 80\% \)
Chọn C.
congdong.edu.vn