Lớp 12 - SBT Hóa học Giải bài 6.80, 6.81, 6.82, 6.83, 6.84, 6.85 trang 66 , 67 Sách bài tập Hóa học 12
Bài 6.80 trang 66 sách bài tập (SBT) Hóa học 12
Xác định các chất trong chuỗi phản ứng :
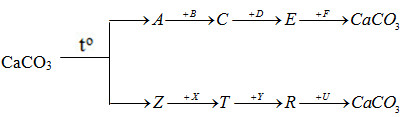
Hướng dẫn trả lời:
A: CaO B: H2O
C: Ca(OH)2 D: HCl
E: CaCl2 F: Na2CO3 Z: CO2
X: Ba(OH)2 T: Ba(HCO3)2
Y: KOH R: K2CO3 U: Ca(NO3)2
Bài 6.81 trang 67 sách bài tập (SBT) Hóa học 12
Xác định các chất trong chuỗi phản ứng sau :
A + B → C + H2O
\(B\buildrel {{t^0}} \over
\longrightarrow C + {H_2}O + D \uparrow \)
D+ A → B hoặc C
Biết D là hợp chất của cacbon. A, B, C là hợp chất của một kim loại, khi đốt nóng cho ngọn lửa màu vàng.
Hướng dẫn trả lời:
A: NaOH B: NaHCO3 C: Na2CO3 D: CO2
Bài 6.82 trang 67 sách bài tập (SBT) Hóa học 12
Cho các chất : MgCO3, MgO, Mg(OH)2, MgCl2, MgSO4. Hãy viết PTHH của các chuỗi phản ứng có thể xảy ra theo sơ đồ:
A ⟶ B ⟶ C ⟶ D ⟶ E
Hướng dẫn trả lời:
Có nhiều chuỗi phản ứng phù hợp sơ đồ trên. Ví dụ :
MgO ⟶ MgCl2 ⟶ MgCO3 ⟶ MgSO4 ⟶ Mg(OH)2
MgO ⟶ MgSO4 ⟶ MgCO3 ⟶ MgCl2 ⟶ Mg(OH)2
MgCO3 ⟶ MgO ⟶ MgCl2 ⟶ MgSO4 ⟶ Mg(OH)2
Mg(OH)2 ⟶ MgCl2 ⟶ MgCO3 ⟶ MgO ⟶ MgSO4
Bài 6.83 trang 67 sách bài tập (SBT) Hóa học 12
Ion Ca2+ có cấu hình electron giống với cấu hình electron của nguyên tử khí hiếm và ion halogen nào ? Viết cấu hình electron của chúng.
Hướng dẫn trả lời:
Cấu hình của ion Ca2+ : 1 s22s22p63s23p6. Giống cấu hình electron của nguy tử khí hiếm đứng trước nó là agon (Ar) và cấu hình electron của ion Cl-
Bài 6.84 trang 67 sách bài tập (SBT) Hóa học 12
Bằng những phản ứng hoá học nào có thể phân biệt được các chất trong mỗi dãy sau ?
a) Các kim loại : Al, Mg, Ba, Na.
b) Các dung dịch muối : NaCl, Ba(NO3)2, Al(SO4)3.
c) Các oxit : CaO, FeO, Al2O3.
d) Các dung dịch : NaNO3, Ca(NO3)2, Al(NO3)3.
Hướng dẫn trả lời:
a) Dùng H2O, nhận biết được 2 nhóm kim loại Na, Ba và Mg, Al. Nhận biết ion Ba2+ trong nhóm ( 1 ) bằng ion CO3 2- . Nhận biết kim loại Al trong nhóm (2) bằng dung dịch NaOH.
b) Nhận biết ion Al3+ bằng dung dịch NaOH, sau đó nhận biết ion Ba2+ bằng dung dịch muối cacbonat, còn lại là dung dịch chứa Na+.
c) Dùng H2O nhận biết CaO, dùng dung dịch NaOH nhận biết A12O3, chất còn lại là FeO.
d) Dùng dung dịch NaOH nhận biết: A1(NO3)3 tạo kết tủa sau đó tan trong dung dịch NaOH dư ; Ca(NO3)2 làm dung dịch vẩn đục, còn lại là NaNO3.
Bài 6.85 trang 67 sách bài tập (SBT) Hóa học 12
Trình bày phương pháp điều chế từng kim loại riêng biệt từ hỗn hợp những chất NaCl, A12O3, MgCO3. Viết các phương trình hoá học.
Hướng dẫn trả lời:
Dùng nước tách được NaCl. Cô cạn dung dịch được NaCl rắn. Điện phân NaCl nóng chảy, được kim loại Na.
Dùng dung dịch NaOH dư, tách được chất rắn MgCO3 và dung dịch NaAlO2. Từ MgCO3 điều chế kim loại Mg theo sơ đồ chuyển hoá sau:
\(MgC{O_3}\buildrel {{t^0}} \over
\longrightarrow MgO\buildrel {{\rm{dd HCl}}} \over
\longrightarrow MgC{l_2}\buildrel {dpnc} \over
\longrightarrow Mg\)
Từ natri aluminat điều chế Al theo sơ đồ chuyển hóa:
\(NaAl{O_2}\buildrel {C{O_2}} \over
\longrightarrow Al{(OH)_3}\buildrel {{t^0}} \over
\longrightarrow A{l_2}{O_3}\buildrel {dpnc} \over
\longrightarrow Al\)
congdong.edu.vn